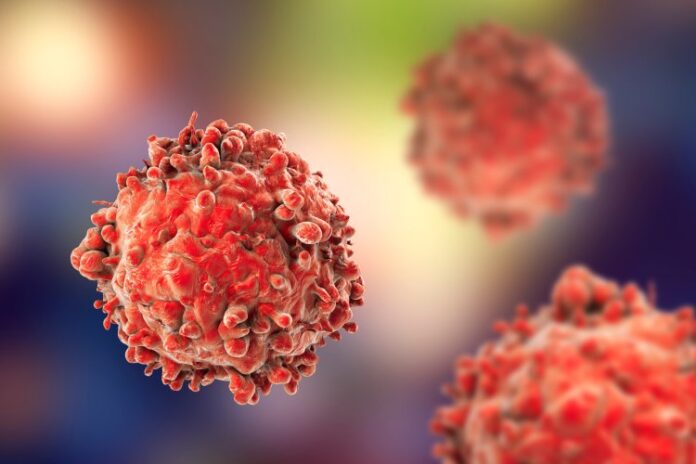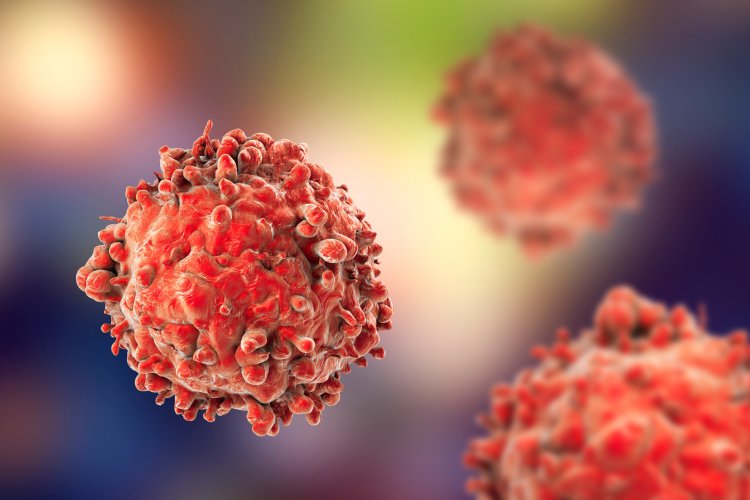
Злокачественные новообразования яичников нередко вырабатывают резистентность к стандартным протоколам лечения. Основной подход включает хирургию и курсы препаратов платины, однако после временного успеха у 80% пациентов наблюдается рецидив в течение года. Ученые нашли объяснение этому явлению, открыв новые пути для оптимизации терапии.
Ключевые открытия ученых ФНКЦ ФХМ и МФТИ
Специалисты ФНКЦ ФХМ им. Лопухина ФМБА России и МФТИ провели детальный анализ на клеточном уровне. Исследование показало: погибающие при химиотерапии злокачественные клетки активно выделяют внеклеточные везикулы. Эти частицы усиливают устойчивость соседних клеток, делая их агрессивнее. Открытие подтверждает, что межклеточная коммуникация играет решающую роль в развитии резистентности.
Новые горизонты в понимании резистентности
Несмотря на прогресс в онкологии, рак яичников сохраняет высокие показатели летальности. Ранее считалось, что устойчивость формируется за счет внутренних мутаций. Но данные секвенирования РНК указали на другой сценарий: выжившие после терапии клетки либо уже присутствуют в опухоли, либо образуются во время лечения. Это открывает возможности для таргетного воздействия на опасные субпопуляции.
Перспективные результаты исследований
«Мы обнаружили, что под действием химиотерапии опухолевые клетки начинают активно обмениваться сигнальными молекулами, — комментирует Виктория Шендер, заведующая лабораторией ФНКЦ. — Анализ секреции in vitro и ex vivo помог выявить ключевые соединения, влияющие на устойчивость». Эти данные позволяют разрабатывать методы блокировки межклеточной коммуникации, повышающие эффективность лечения.
Прорыв в понимании механизмов химиотерапии
«Химиотерапия требует особой точности — введение максимально возможной дозы препарата ограничено его токсичностью. Некоторые опухолевые клетки образуют сложные структуры, такие как сфероиды или фиброзные капсулы, что создаёт барьер для лекарств. Интересно, что даже погибающие клетки вносят вклад в развитие опухоли, выделяя молекулы, которые стимулируют рост соседних клеток. Изучение этих процессов in vivo особенно эффективно на примере карцином яичников», — подчеркнул Георгий Арапиди, заведующий лабораторией системной биологии ФНКЦ ФХМ им. акад. Ю.М. Лопухина, доцент МФТИ.
Асцит как ключ к разгадке
При раке яичников часто развивается асцит — скопление жидкости в брюшной полости. В таких случаях химиотерапия становится первым этапом лечения, уменьшая объём асцита до 80%. Однако в этой жидкости формируется особая микросреда, где опухолевые, иммунные и стромальные клетки взаимодействуют, усиливая устойчивость к терапии и подавляя иммунитет. Учёные исследовали парные образцы асцитической жидкости до и после химиотерапии, чтобы раскрыть секреты этой динамики.
Открытие белков-защитников
«Мы обнаружили, что после терапии асцит обогащается белками, регулирующими сплайсинг РНК, которые обычно находятся в ядре. Эти компоненты делают опухолевые клетки более агрессивными, активируя гены репарации ДНК и клеточного цикла. Эксперименты in vitro подтвердили: везикулы с элементами сплайсосомы ускоряют восстановление ДНК, помогая клеткам противостоять цисплатину», — рассказала Виктория Шендер. Это открытие объясняет, как опухоль адаптируется к лечению.
Перспективы для персонализированной терапии
Расшифровка сигнальных сетей в микросреде опухоли открывает новые горизонты. Управление этими механизмами или их блокировка могут значительно повысить эффективность химиотерапии. Учёные уверены: дальнейшие исследования помогут создать адресные методы лечения, превращая научные находки в реальные инструменты борьбы с раком.
Прорыв в исследовании терапии онкологических заболеваний
Крупномасштабное международное исследование объединило усилия ведущих научных центров, включая Федеральный научно-клинический центр физико-химической медицины, МГУ, Институт биофизики будущего МФТИ и университеты из России, Китая и Франции. Совместная работа позволила раскрыть новые механизмы взаимодействия раковых клеток, открывающие перспективы для создания инновационных методов лечения.
Научные открытия в борьбе с раком яичников
Исследовательская группа под руководством В.О. Шендера обнаружила уникальный клеточный механизм: компоненты сплайсосомы, выделяемые при терапии, усиливают выживаемость злокачественных клеток. Это открытие, опубликованное в Nature Communications, создаёт основу для разработки таргетированных препаратов, способных блокировать патологическую коммуникацию между клетками и повышать эффективность лечения.
Статья: Shender, V.O., Anufrieva, K.S., Shnaider, P.V. et al. Therapy-induced secretion of spliceosomal components mediates pro-survival crosstalk between ovarian cancer cells. Nat Commun 15, 5237 (2024)
Информация предоставлена Центром научной коммуникации МФТИ
Источник фото: ru.123rf.com
Источник: scientificrussia.ru